1.- Cadena más larga: metano, etano, propano, butano, pentano,...
2.- Las ramificaciones como radicales: metil(o), etil(o),...
3.- Se numera para obtener los números más bajos en las ramificaciones.
4.- Se escriben los radicales por orden alfabético y con los prefijos di-, tri-, ... si fuese necesario.
5.- Los hidrocarburos cíclicos anteponen el prefijo ciclo-
Propiedades físicas
CH4 + Cl2 ----> CH3Cl + HCl
AlCl3
CH3CH2CH2CH3 ------> CH3CH(CH3)2
Obtención de alcanos
- Hidrogenación de alcanos:
Ni
CH3CH=CHCH3 -----> CH3CH2CH2CH3
- Reducción de haluros de alquilo: Zn
2 CH3CH2CHCH3 ------> 2 CH3CH2CH2CH3 + ZnBr2
Nomenclatura
1.- Seleccionar la cadena principal: mayor número de dobles enlaces y más larga. Sufijo -eno.
2.- Numerar para obtener números menores en los dobles enlaces.
Propiedades físicas
CH3-CH=CH-CH3 + XY ------> CH3-CHX-CHY-CH3
entre ellas destacan la hidrogenación, la halogenación, la hidrohalogenación y la hidratación. En estas dos últimas se sigue la regla de Markovnikov y se forman los derivados más sustituidos, debido a que el mecanismo transcurre mediante carbocationes y se forma el carbocatión más estable que es el más sustituido.Obtención de alquenos
CH3-CHX-CHY-CH3 ------> CH3CH=CHCH3 + XY
entre ellas destacan la deshidrogenación, la deshalogenación, la deshidrohalogenación y la deshidratación. Las deshidratación es un ejemplo interesante, el mecanismo transcurre a traves de un carbocatión y esto hace que la reactividad de los alcoholes sea mayor cuanto más sustituidos. En algunos casos se producen rearreglos de carbonos para obtener el carbocatión más sustituido que es más estable. De igual modo el alqueno que se produce es el más sustituido pues es el más estable. Esto provoca en algunos casos la migración de un protón.ALQUINOS
1.- Se consideran como dobles enlaces al elegir la cadena principal.
2.- Se numera dando preferencia a los dobles enlaces.
HIDROCARBUROS AROMATICOS
Aromáticos
El benceno es el principal ejemplo de un compuesto aromático. Para que un hidrocarburo sea aromático, debe presentar un ciclo de seis miembros, y dentro de este ciclo, tres dobles enlaces alternados. El naftaleno C10H8 es también aromático, y es el componente principal de la naftalina. Por otro lado, la vainillina, presente en la vainilla, presenta también un anillo aromático.
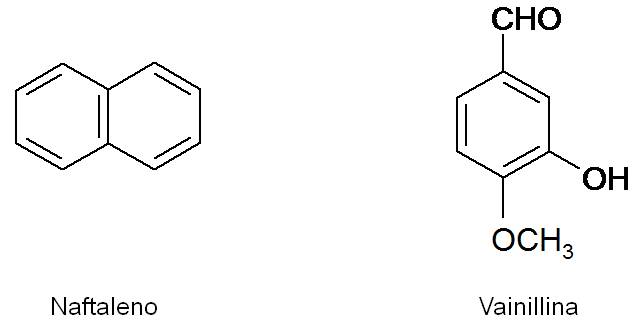
Los compuestos aromáticos muestran una gran estabilidad y son poco reactivos. Asimismo, poseen un olor característico
ALCOHOLES
Los alcoholes poseen un enlace C-O-H, es decir, se tiene un oxígeno unido tanto a un carbono como a un hidrógeno por medio de enlaces simples. En forma abreviada, lo representamos así:
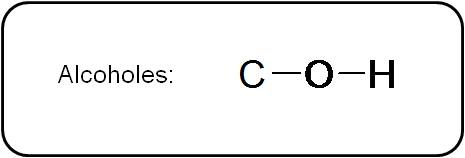
Los alcoholes que no tienen muchos átomos de carbono son solubles en agua y, por lo general, son líquidos a temperatura ambiente (o tienen un punto de ebullición relativamente alto). Esto se debe a que son capaces de formar enlaces de hidrógeno.
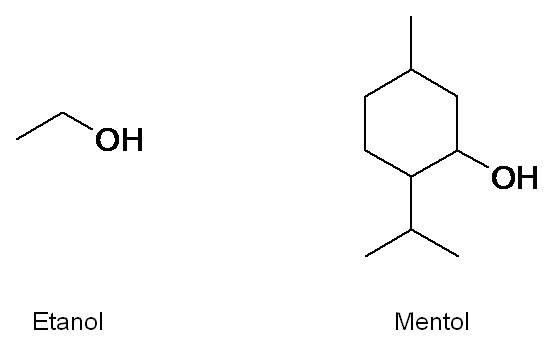
El etanol C2H5OH es uno de los alcoholes más conocidos por nosotros. Lo usamos como desinfectante y es el componente principal de las bebidas alcohólicas. Otro alcohol es el mentol, presente en el aceite de menta, usado en cremas dentales por su olor y sabor característico.
ETERES |
Los éteres poseen un oxígeno unido a dos átomos de carbono por medio de enlaces simples. En general:
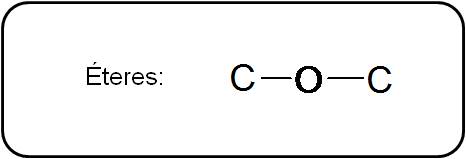
Los éteres tienen punto de ebullición menor que los alcoholes, puesto que no presentan fuerzas intermoleculares de enlace de hidrógeno. Asimismo, debido a esto, son muy poco solubles en agua.
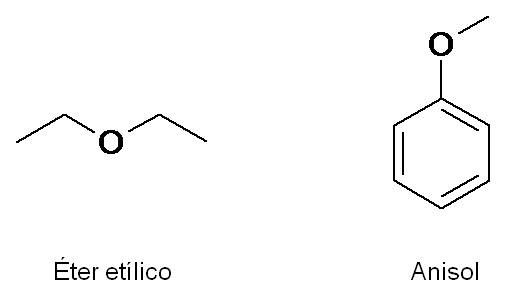
El éter etílico es muy conocido como solvente y fue usado durante muchos años como anestésico, debido a su peculiar olor (que da sueño). El anisol, por otro lado, es el responsable del olor del anís.
ALDEHIDOS Y CETONAS
Los aldehídos y cetonas presentan un doble enlace entre un carbono y un oxígeno (denominado grupo carbonilo). La diferencia entre ellos radica en los átomos adyacentes al carbono en mención. En general:
Observa las semejanzas y diferencias entre un aldehído y una cetona: ambos tienen un grupo carbonilo (C=O). El aldehído tiene, unido al carbono del carbonilo, un carbono y un hidrógeno, mientras que una cetona tiene unido sólo átomos de carbono.
Los aldehídos y cetonas con pocos átomos de carbono son solubles en agua. Por lo general son líquidos a temperatura ambiente, aunque tienen bajo punto de ebullición.
El cinamaldehído es un aldehído que se encuentra en la canela y es responsable del olor. La acetona es la cetona más simple, y se usa como disolvente (por ejemplo, para quitar el esmalte de uñas).
